همشهری آنلاین -یکتافراهانی : تحقیقات اخیر در خصوص ترکیب علم با هوش مصنوعی به رهبری دکتر رافائل برناردی در دانشگاه آبرن و منتشر شده در مجله انجمن شیمی آمریکا به چالش جدیدی از طریق ترکیب هوش مصنوعی و شبیه سازی دینامیک مولکولی پرداخته و مسیری امیدوارکننده برای درمان های شخصی سرطان ارائه داده است.
سنگ بنای بسیاری از درمان های ایمنی
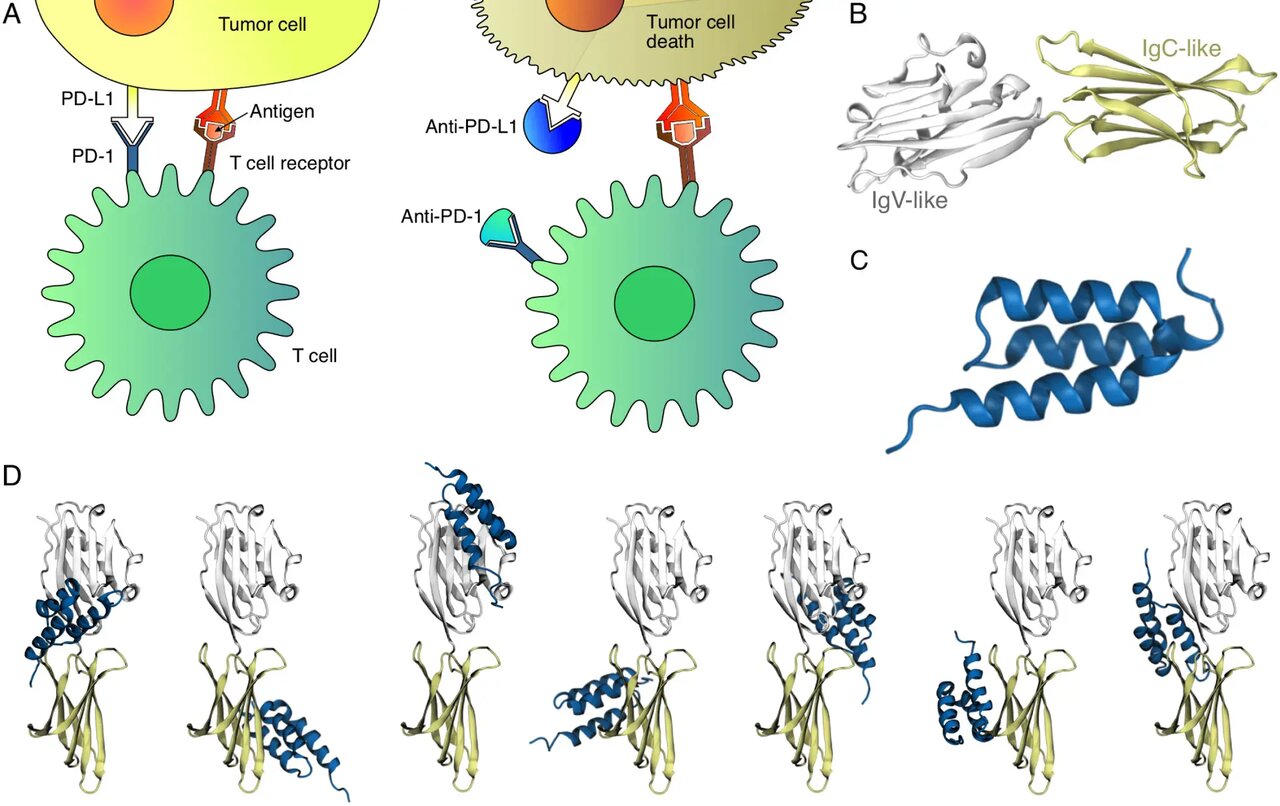
هدف قرار دادن پروتئین PD-L۱ سنگ بنای بسیاری از درمان های ایمنی سرطان است. PD-L۱ به سلولهای سرطانی اجازه میدهد تا با سرکوب پاسخهای ایمنی از تشخیص ایمنی فرار کنند.
داروهای مسدود کننده PD-L۱ مانند پمبرولیزوماب، سیستم ایمنی را برای حمله به تومورها آزاد می کند. با وجود این، پیشبینی دقیق مکانهای اتصال برای چنین درمانهایی همچنان یک چالش بزرگ است.
تقویت ابزارهای هوش مصنوعی با شبیهسازی دینامیک مولکولی
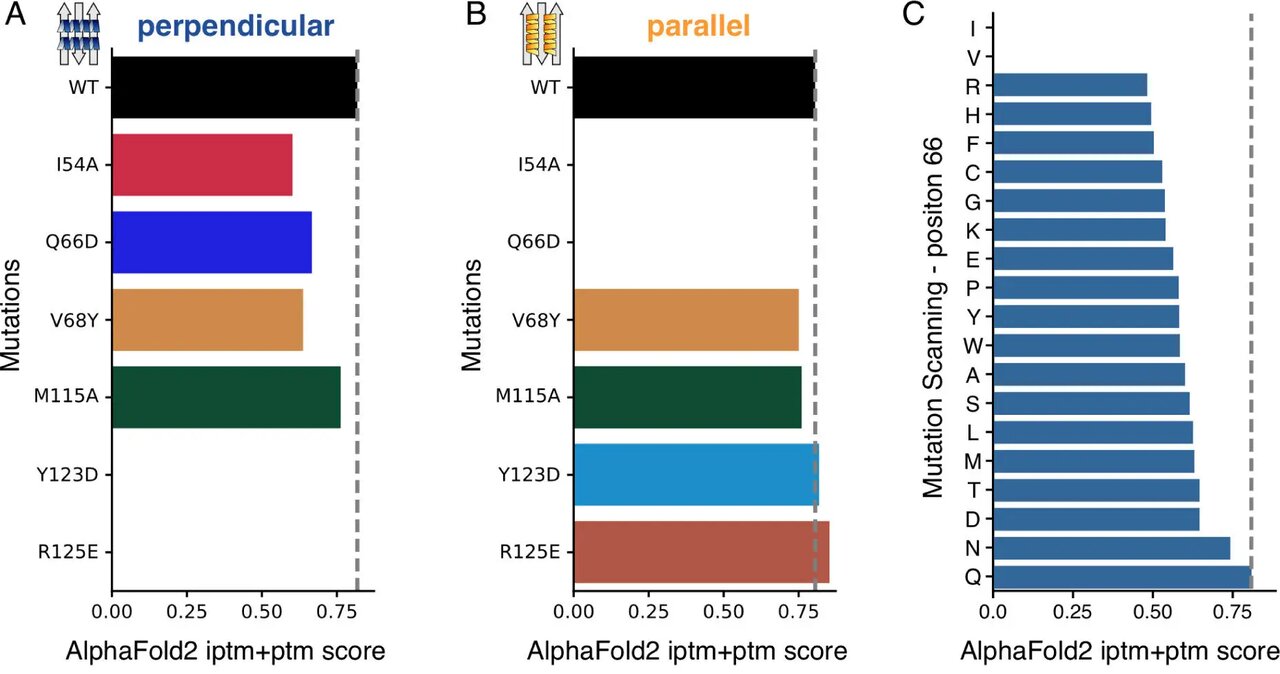
تیم دکتر برناردی با تقویت ابزارهای هوش مصنوعی با شبیهسازی دینامیک مولکولی و تجزیه و تحلیل شبکه پویا با این مشکل مقابله کردند. روشهای سنتی مبتنی بر هوش مصنوعی، از جمله AlphaFold۲، در تمایز بین مدلهای اتصال موثر اما ناکافی بودند.
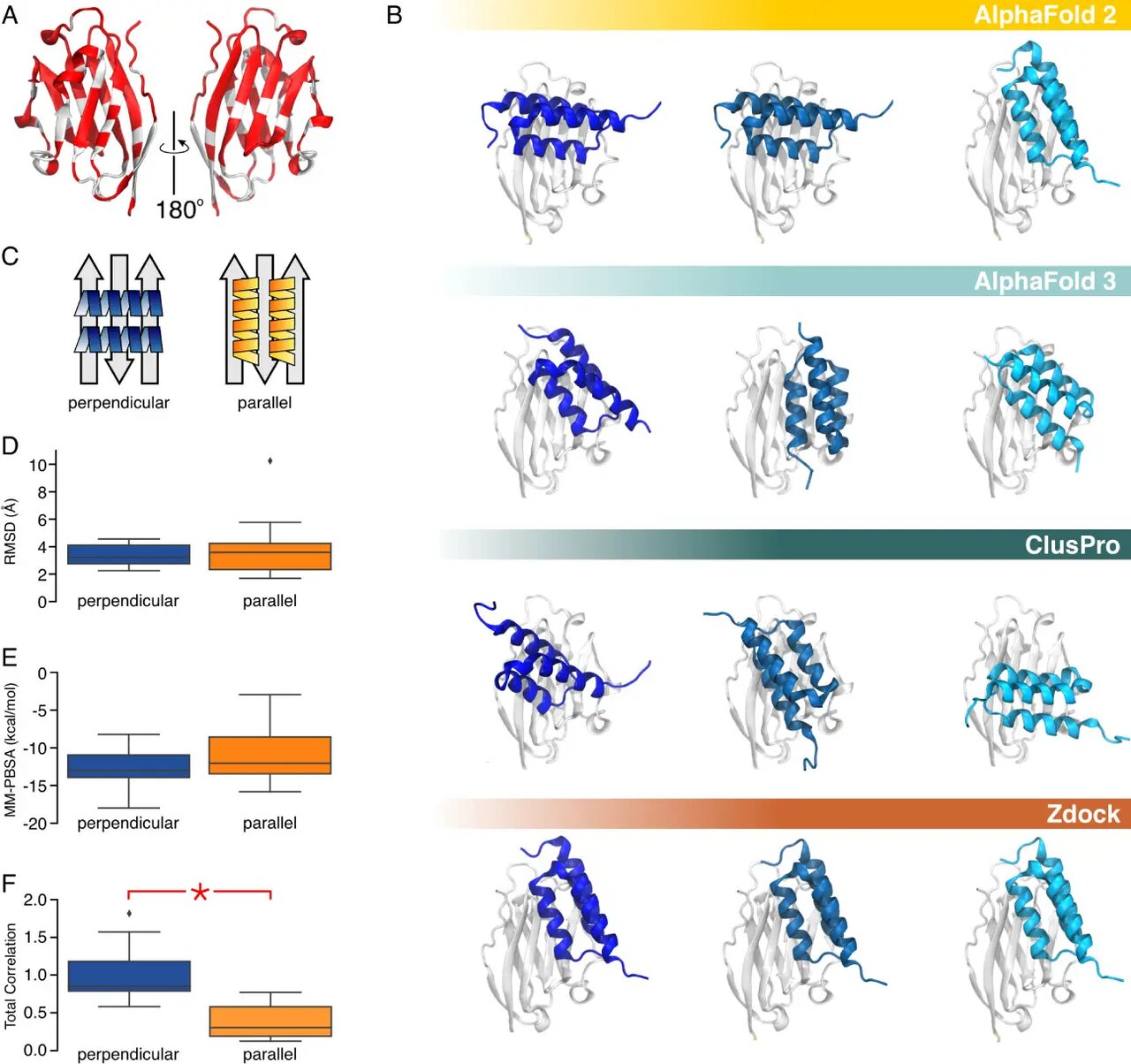
رویکرد یکپارچه تیم بسیار مهم بود و نشان داد که حالت اتصال عمودی مجتمعهای PD-L۱: Affibody به طور قابلتوجهی پایدارتر از پیکربندی موازی است. این پیشبینی از طریق تکنیکهای تجربی پیشرفته، از جمله طیفسنجی جرمی پیوند متقابل و اسکن جهشی مبتنی بر توالییابی نسل بعدی تأیید شد.
بیشتر بخوانید :
مرز بعدی در درمان سرطان
این مطالعه شامل محققانی از دانشگاه Auburn، دانشگاه بازل و ETH زوریخ بود. به گفته دکتر برناردی، استفاده از ابزارهای محاسباتی برای مهندسی پروتئین ها، مرز بعدی در درمان سرطان را نشان می دهد. این همکاری بین رشتهای در اصلاح پیشبینیهای محاسباتی با اعتبار تجربی بسیار مهم بود.
به گزارش سایت thebrighterside محقق اصلی این پروژه، دکتر دیگو گومز عقیده دارد : این کار هم افزایی بین نوآوریهای محاسباتی و تکنیکهای تجربی را به نمایش میگذارد که باعث پیشرفت در درمان سرطان میشود.
این تیم با استفاده از منابع پیشرفته مانند سیستمهای NVIDIA DGX، قابلیتهای ابزارهایی مانند NAMD و VMD را ارتقا داد و بر نقش محاسبات با کارایی بالا در بیوفیزیک مدرن تأکید کرد.
تقویت هوش مصنوعی توسط شبکه پویا
تجزیه و تحلیل شبکه پویا سنگ بنای این تحقیق است. محققان با استفاده از این تکنیک در مسیرهای دینامیک مولکولی تولید شده از ساختارهای AlphaFold۲Multimer، پایدارترین پیکربندیهای اتصال را شناسایی کردند. قابل توجه است که AlphaFold۳ نتوانست وضعیت اتصال عمود بر هم را پیشبینی کند که محدودیتهای مدلهای فقط هوش مصنوعی و نیاز به روشهای یکپارچه را برجسته میکند.
پیامدهای گسترده تر برای پزشکی
در حالی که این مطالعه بر روی PD-L۱ متمرکز بود، پیامدهای آن بسیار فراتر از ایمونوتراپی سرطان است. روشهای توسعهیافته را میتوان روی پروتئینهای دیگر اعمال کرد و راه را برای درمانهای جدید برای بیماریهای مختلف از جمله شرایط خودایمنی هموار کرد. علاوه بر این، این رویکرد میتواند با رفع محدودیتهای روشهای تجربی سنتی، کشف دارو را تسریع کند و هزینهها را کاهش دهد.
به گفته دکتر گومز کاربردهای بالقوه روشهای ما بسیار گسترده است؛ از شناسایی اهداف دارویی در بیماریهای مختلف گرفته تا انقلابی کردن پزشکی شخصیشده.
آینده امیدوارانه تر در درمان های شخصی و مقرون به صرفه
همان گونه که مبارزه با سرطان ادامه دارد، ادغام هوش مصنوعی با تجزیه و تحلیل شبکه پویا و دینامیک مولکولی احتمالا نقشی اساسی در نوآوری درمانی ایفا خواهد کرد. تیم بیوفیزیک دانشگاه آبرن نشان می دهد که چگونه همکاری در فیزیک، شیمی و زیست شناسی می تواند باعث پیشرفت معنادار شود.
این تحقیق نه تنها درمان سرطان را پیش می برد، بلکه بر پتانسیل گسترده تر ابزارهای محاسباتی در پزشکی نیز تأکید می کند. همان طور که تیم دکتر برناردی به اصلاح این تکنیک ها ادامه می دهد، آینده درمان های شخصی و مقرون به صرفه به طور فزاینده ای امیدوارکننده به نظر می رسد.
































نظر شما